Jämförande värdering av NOAK vid förmaksflimmer
Sammanfattning
Fyra direktverkande Non-vitamin K Orala Antikoagulantia (NOAK) – trombinhämmaren dabigatran (Pradaxa) samt faktor Xa (FXa)-hämmarna rivaroxaban (Xarelto), apixaban (Eliquis) och edoxaban (Lixiana) – finns nu tillgängliga för prevention av stroke vid icke-valvulärt förmaksflimmer (FF). Liksom för warfarin bör NOAK förskrivas med god kännedom om deras egenskaper samt med en god uppföljning av behandlingen. I Kloka Listan 2017 rekommenderas apixaban i första hand och warfarin eller dabigatran i andra hand. För patienter med mekanisk klaffprotes eller signifikant mitralisstenos ska warfarin användas.
Alla fyra NOAK har visat likartat eller bättre förebyggande av stroke och likartad eller lägre risk för allvarlig blödning jämfört med warfarin (PK(INR)-mål 2,0–3,0) i multinationella studier med 6 000–9 000 FF-patienter per behandlingsgrupp och 1,6–2 års medianuppföljning. Jämfört med warfarin var risken för hjärnblödning lägre med alla NOAK men den absoluta skillnaden är liten. Risken för allvarlig gastrointestinal blödning var högre med dabigatran och edoxaban i höga doseringar samt med rivaroxaban, men ej med apixaban. Andra studier har visat att apixaban och warfarin ger en väsentligt bättre strokeprofylax än lågdos ASA utan väsentlig skillnad i risken för allvarliga blödningar. FF-patienter med ökad risk för stroke bör därför erbjudas behandling med ett oralt antikoagulantium (OAK) i stället för ASA.
I de stora studierna har warfarinbehandlingens kvalitet föranlett tveksamhet om studiernas generaliserbarhet till länder med välskött warfarinbehandling såsom Sverige. Socialstyrelsen har 2015, liksom American Heart Association (AHA) 2014, valt att rekommendera warfarin och NOAK med samma prioritet medan det Europeiska kardiologsällskapet (ESC) rekommenderade NOAK före warfarin redan 2012. Stora observationsstudier har visat att NOAK kan ges med god säkerhet och effektivitet i klinisk rutin och detta bekräftas även av data från vår egen sjukvård. I klinisk praxis är NOAK enklare att administrera då frekvent provtagning inte behövs såsom med warfarin. Självmätning och egenkontroll finns dock för warfarin. Vid konvertering av FF är tidsvinsten med NOAK i stället för warfarin värdefull.
NOAK är, till skillnad från warfarin, direktverkande hämmare av trombin (FII) eller FXa. Effekten av NOAK är direkt beroende av plasmahalten och kommer inom ett par timmar efter den första dosen och försvinner snabbare än för warfarin efter den sista dosen.
NOAK vid nedsatt njurfunktion
Vid val av OAK bör komorbiditet, övrig läkemedelsbehandling och patientens önskemål beaktas. Alla NOAK kan behöva dosreduceras vid sänkt njurfunktion och de bör förskrivas med stor försiktighet vid eGFR <25–30 ml/min eftersom sådana patienter inte är studerade. Dabigatran har det största (80 procent) och apixaban det minsta (27 procent) njurfunktionsberoendet för sin eliminering vilket särskilt bör beaktas för patienter som är äldre (≥80 år) och/eller har sänkt njurfunktion.
Rivaroxaban doseras x 1 trots den kortaste halveringstiden av alla NOAK medan dabigatran och apixaban doseras x 2. Det finns både för- och nackdelar med en endosregim som kan vara bekväm för patienten men leda till sämre tromboemboliskydd vid uteblivet intag.
Rivaroxaban var non-inferior till warfarin i den stora ROCKET-AF studien men kvaliteten i den jämförda warfarinbehandlingen var låg – sämre än den som övriga NOAK jämfördes med. Dabigatran i normaldosen 150 mg x 2 gav det bästa skyddet mot ischemisk stroke medan apixabanbehandlade patienter hade den lägsta risken för allvarlig blödning; samtliga NOAK minskade risken för hemorragisk stroke jämfört med warfarin. Apixaban rekommenderades i första hand jämte warfarin i Kloka Listan 2015 och dabigatran rekommenderades i andra hand. En nätverksmetaanalys av de pivotala NOAK-studierna som kom 2016 konkluderade att apixaban hade ett försteg före dabigatran och rivaroxaban.
Apixaban vanligast vid nyinsättning
Apixaban dominerar nu nyinsättningarna av OAK vid FF (Figur 1) och våra uppföljningar av behandlingsresultat med NOAK är betryggande. Persistensen med OAK-behandling i SLL var mycket god (88 procent efter ett år och 83 procent efter två år) och bättre med warfarin och apixaban än med rivaroxaban och dabigatran. Olika studier av persistens och adherens rapporterar skilda resultat beroende på faktiska skillnader och/eller metodologiska problem.
Kliniska utfall hos alla FF-patienter som påbörjade OAK-behandling 2012–2015 i SLL var minst lika goda med NOAK som med warfarin, även i vulnerabla subgrupper såsom patienter ≥80 år eller de som haft en tidigare allvarlig blödning. Dosreduktioner av NOAK var mycket vanligare i SLL än i de stora studierna och förefaller vara adekvata bland de äldre men kanske inte hos yngre patienter.
Allt fler observationella studier från olika register i Europa och USA bekräftar bilden att NOAK skyddar minst lika väl mot tromboemboli som warfarin (dagibatran något bättre) men att NOAK (särskilt apixaban) har fördelar vad avser risker för allvarlig blödning.
Interaktioner med andra läkemedel
Jämfört med warfarin uppvisar NOAK en lägre risk för läkemedelsinteraktioner men kunskaperna om deras kliniska betydelse är ännu ofullständig. Alla NOAK interagerar med ett flertal läkemedel via P-glykoprotein (P-Gp), bland annat flera antiarytmika som används vid förmaksflimmer. Dessutom finns interaktioner via andra mekanismer såsom CYP3A4 med rivaroxaban och apixaban. Dabigatran och edoxaban är de NOAK som har minst läkemedelsinteraktioner. Samtidig trombocythämmande behandling ökar blödningsrisken och kombination av NOAK med potenta ADP-receptorhämmare som tikagrelor (Brilique) rekommenderas inte. Andra medel som kan öka blödningsrisken (till exempel NSAID, SSRI) bör om möjligt undvikas.
En specifik antidot finns nu för dabigatran (Praxbind). Protrombinkomplex-koncentrat kan reversera effekter av FXa-hämmarna (liksom av warfarin) men erfarenheterna av detta är mycket begränsade och specifika antidoter mot FXa-hämmarna är ännu ej tillgängliga.
Rutinmässig monitorering av NOAK-effekter behövs inte men speciella tester som finns tillgängliga i SLL kan användas för bedömning av behandlingsintensiteten i akuta situationer och även för dosjustering. En klok användning av validerade tester torde i framtiden kunna leda till en ännu effektivare och säkrare NOAK-behandling. Erfarenheterna av att hantera allvarliga blödningar och invasiva ingrepp under NOAK-behandling är ännu begränsade.
Alla som kan komma i kontakt med NOAK-behandlade patienter i akuta situationer och inför interventioner med ökad risk för allvarlig blödning bör ha god kunskap om läkemedlen. Patienterna ska vara välinformerade och väl uppföljda. ”AK-brickor” ska erbjudas även NOAK-behandlade patienter och AK-varning ska föras in i journalen.
Läkemedelskommitténs uppdrag är att ge rekommendationer som syftar till att främja en säker, rationell och kostnadseffektiv läkemedelsanvändning, att vara ett stöd för vården – i synnerhet primärvården där de flesta FF-patienter handläggs – och ge råd om kloka val när det finns ett flertal liknande alternativ för behandling. Enkelheten med NOAK – jämfört med warfarinbehandling är en fördel som gör att vi nu, med stöd från flera stora observationella studier och även uppföljningar i SLL, kan rekommendera apixaban i första hand och dabigatran eller warfarin i andra hand i Kloka Listan. Man bör notera att enkelheten med NOAK kan vara skenbar och att warfarin fortsatt ska användas i vissa situationer. Behandlingen ska anpassas till den aktuella patientens förutsättningar och önskemål och därför frångås Kloka Listans rekommendationer ibland.
Man bör inte ändra en välfungerande antikoagulantiabehandling utan goda skäl. Förskrivare ska vara väl förtrogna med preparaten som ordineras och det är viktigt med en god uppföljning av behandlingen oavsett val av läkemedel.
All antikoagulantiabehandling innebär en balansgång mellan riskerna för tromboembolisk händelse och allvarlig blödning. NOAK ska hanteras med samma respekt som warfarin.
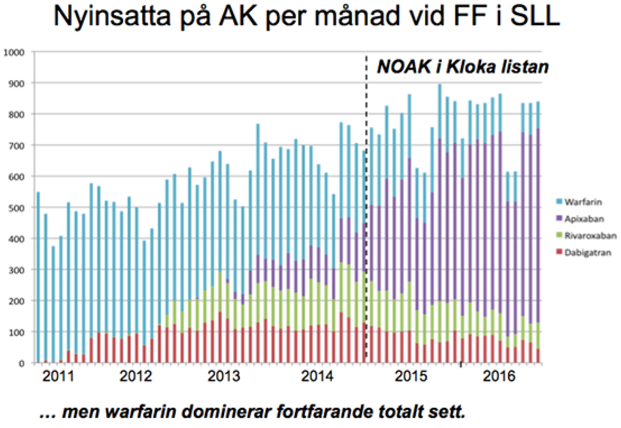
Figur 1. Nyinsättningarna av OAK har ökat från cirka 500/månad 2011 till bortåt 900/månad. NOAK gick om warfarin sent 2014 och apixaban dominerar nyinsättningarna efter rekommendation i Kloka Listan. Totalt behandlas fortfarande fler FF-patienter med warfarin än med NOAK.
Bakgrund
Förmaksflimmer (FF) är vanligt förekommande med en prevalens av minst 3 procent i den vuxna befolkningen och prevalensen ökar med stigande ålder till 10–15 procent hos individer ≥75 år [1]. Strokerisken vid FF ökar markant vid högre ålder. I SLL har vi sett en markant ökning av antalet patienter med FF-diagnos i VAL-databasen (som inkluderar primärvården) från drygt 43 000 patienter med en icke-valvulär FF-diagnos de senaste fem åren 2010 till >50 000 patienter 2016 (efter exklusion av nyligen in- eller utflyttade samt avlidna personer). Det finns dessutom ett antal asymtomatiska, ännu icke diagnosticerade FF-patienter. Strokeprofylax med warfarin är väl inarbetat sedan länge. Underbehandling med OAK och överbehandling med ASA har varit viktiga frågor i SLL liksom i andra regioner i Sverige och i andra länder. Införandet av NOAK underlättar för fler patienter med FF att få en adekvat behandling.
Risken att drabbas av tromboemboliska komplikationer, främst ischemisk stroke, ska skattas hos varje FF-patient och vägas mot blödningsrisken inför ställningstagande till att erbjuda OAK-behandling. Europeiska [2,3] och svenska [4] riktlinjer rekommenderar användning av CHA2DS2VASc-skalan som är återgiven i vår ”Lathund” [5] och i Viss. Indikation för AK-behandling anses nu finnas vid CHA2DS2VASc ≥2 för män och ≥3 för kvinnor; behandling kan övervägas vid CHA2DS2VASc =1 för män och 2 för kvinnor (poängen för kvinnligt kön påverkar således inte längre ställningstagandet till OAK-behandling) [3]. Det är viktigt att erbjuda patienter med en betydelsefull risk (och utan kontraindikationer) OAK-behandling men det är även viktigt att inte överbehandla patienter med låg risk. Därvid är det av intresse att den ”1-poängsfaktor” i CHA2DS2VASc som medför en tydligt ökad strokerisk är ålder 65–74 år (relativ risk cirka 3) medan övriga riskindikatorer som ger 1 poäng medför betydligt mindre riskökningar [3]. Således ger åldern en viktig vägledning vid ställningstagande till eventuell behandling av lågriskpatienter [5].
Vid ställningstagande till OAK-behandling ska risken att drabbas av allvarlig blödning och patientens egna önskemål vägas in. HAS-BLED skalan som förordats i tidigare riktlinjer har ersatts av en rekommendation att utvärdera och åtgärda påverkbara riskfaktorer för blödning [3,5]. Riskerna för tromboembolism och allvarlig blödning samvarierar påtagligt men minskningen av strokerisken är i de flesta fall väsentligt större än ökningen av blödningsrisken med OAK-behandling.
I SLL hämtade 74 procent av alla patienter med icke-valvulärt FF ut något OAK under 2016 (upp från 51 procent 2011). Bland de med tydlig indikation för OAK-behandling (CHA2DS2VASc ≥2) ökade under dessa år OAK-behandlingen från 54 procent till 79 procent, vilket motsvarar Socialstyrelsens arbiträra mål om 80 procent av dessa patienter [4]. 2016 hämtade 19 500 FF-patienter ut warfarin och 17 000 något NOAK. Apixaban rekommenderades jämte warfarin i första hand och dabigatran i andra hand i Kloka Listan 2015. Mot slutet av 2015 kom nyinsättningarna av OAK att domineras av apixaban och den trenden har förstärkts (Figur 1); NOAK blir snart vanligare än warfarin. Lathunden ”Antikoagulantiabehandling vid förmaksflimmer Pdf, 645.6 kB.” [5] har uppdaterats med aktuella råd och rekommendationer. Skriften om ”Orala antitrombotiska läkemedel vid blödning och kirurgi” [6] är även uppdaterad.
Strokeprofylaxen är betydligt bättre med warfarin än med ASA
Strokeprofylax vid icke-valvulärt FF har för warfarin dokumenterats jämfört med placebo i äldre studier som visar mycket stora behandlingsvinster i en metaanalys som omfattade 2 900 patienter [7]. Enligt intention-to-treat analyser reducerades strokerisken med 64 procent och med fullföljd god behandling minskade den med mer än 80 procent [7,8]. Warfarin ger således ett mycket effektivt skydd mot stroke och är jämförelsepreparatet i NOAK-studierna. När det är viktigt med en optimal intensitet i behandlingen är warfarin ett utmärkt alternativ som genom monitoreringen kan doseras för bästa balans mellan tromboemboliprofylax och blödning.
ASA ger en väsentligt sämre strokeprofylax vid FF med endast cirka 20 procents riskreduktion jämfört med placebo [7,8]. Trombocythämning påverkar framför allt arteriell trombos varför den effekt man ändå ser kan bero på en reduktion av icke-emboliska stroke. Jämfört med ASA ger OAK-behandling med warfarin [7,9] eller apixaban [10] en halvering av risken att drabbas av stroke utan signifikant fler allvarliga blödningar. ASA bör därför inte erbjudas i stället för warfarin eller NOAK och är i Kloka Listan 2017 inte rekommenderat på indikationen FF. Nyinsättningarna av ASA vid förmaksflimmer avtar kraftigt (från 400/mån 2011 till 50/mån 2016) men vi har fortfarande för många FF-patienter som behandlas med ASA i stället för OAK.
Jämförelse av NOAK
I Sverige används fyra NOAK med delvis skilda egenskaper – trombinhämmaren dabigatran (Pradaxa) [11,12] samt FXa-hämmarna rivaroxaban (Xarelto) [11,13], apixaban (Eliquis) [11,14] och edoxaban (Lixiana) [11,15].
Samtliga NOAK är direktverkande varför effekten kommer snabbt (inom timmar) efter första dosen. Effekten är relaterad till den aktuella plasmahalten av läkemedlet och avtar relativt snabbt (med vissa skillnader mellan läkemedlen och mellan patienter) efter den sista dosen. För samtliga NOAK anges i Fass att doseringarna bör sänkas för vissa patientkategorier men att monitorering av effekten inte behövs.
Pivotala NOAK-studier
De nya medlen har var sin multinationella kliniska prövning [16-19] som jämför utfall avseende tromboemboli och allvarliga blödningar med warfarinbehandling (PK(INR)-mål 2,0–3,0) vid FF. NOAK-studierna har visat likartad eller bättre förbyggande av stroke och likartad eller lägre risk för blödning jämfört med warfarin. För apixaban finns även jämförelsen med ASA [10]. Samtliga studier visar färre hemorragiska stroke och intrakraniella blödningar med NOAK än med warfarin. Intrakraniell blödning är en sällsynt men allvarlig komplikation varför denna fördel med NOAK är viktig även om de absoluta skillnaderna mellan NOAK och warfarin är små. Metaanalyser har visat en bättre överlevnad med NOAK jämfört med warfarin vilket delvis kan bero på färre intrakraniella blödningar. Direkt trombinhämning medför en ökad risk för hjärtinfarkt jämfört med warfarinbehandling [16,20]; risken är inte ökad med FXa-hämmarna [17-19]. Risken att drabbas av allvarlig gastrointestinal blödning var högre med dabigatran eller edoxaban i de högre normaldoserna [16,19] och med rivaroxaban [17], men inte med apixaban [18]. De pivotala NOAK-studierna skiljer sig en del i upplägg (patientselektion, blindning, analysstrategier, med mera) vilket försvårar indirekta jämförelser av de olika medlen. Meta-analyser av de pivotala FF-studierna visar att NOAK som grupp minskar risken för stroke, framför allt hemorragisk stroke och död oavsett orsak jämfört med warfarin men – med undantag för apixaban – ökar risken för gastrointestinal blödning [21,22]. Låg NOAK-dosering minskade risken för blödning men ökade risken för ischemisk stroke [22]. En ”network meta-analysis” konkluderade att apixaban hade den bäst effekt- och säkerhetsprofil bland aktuella NOAK [23].
Studierna är multinationella och kvaliteten av warfarinbehandlingen i kontrollgrupperna har varit suboptimal med medel-TTR (Time in Therapeutic Range) som lägst 55 procent i ROCKET AF studien. Vissa regioner hade extremt dålig warfarinbehandling med medel-TTR <50 procent även i de dubbelblinda studiena där warfarin doseras av studieledningen. En warfarinbehandling med medel-TTR >70 procent ger FF-patienterna en väsentligt bättre strokeprofylax och överlevnad än en behandling med lägre TTR [24,25]. Detta har betydelse för värderingen av NOAK:s effekter och säkerhet jämfört med warfarin ur vårt perspektiv. Sverige låg i topp avseende medel-TTR i NOAK-studierna (75–80 procent) och i de regionala subgruppsanalyserna var NOAK inte överlägsna warfarin i Västeuropa i någon av studierna. Från Auricula har rapporterats ett medel-TTR på 77,4 procent hos FF-patienterna [25] samt i låga frekvenser av ischemisk stroke/TIA (1,54 procent/år), intrakraniella blödningar (0,41 procent/år) och gastrointestinala blödningar (0,67 procent/år) hos alla FF-patienter oavsett risknivå [25,26]. I meta-analysen av Ruff et al fann man att allvarlig blödning var lägre med NOAK jämfört med warfarin om center-baserade TTR var <66 procent men inte om de var ≥66 procent [22]. En metaanalys av regionala skillnader i effekt och säkerhet visar att NOAK är likvärdiga med warfarin avseende strokeprevention men ger en lägre blödningsrisk i Europa [27].
Övrig studierelaterad information av intresse
Det finns ett stort antal publicerade subgruppsanalyser från RE-LY (dabigatran), ROCKET AF (rivaroxaban), ARISTOTLE och AVERROES (apixaban) samt ENGAGE AF-TIMI 48 (edoxaban) vilka rapporterar utfall i relation till till exempel njurfunktion, riskskattningar eller tidigare genomgången stroke. Någon detaljerad diskussion av alla dessa substudier inkluderas inte här. För både dabigatran [28] och apixaban [29] kan man notera att skillnaderna i effekt och säkerhet i jämförelse med warfarin minskar eller försvinner med en bättre TTR för de warfarinbehandlade patienterna.
Observationella studier som jämför NOAK och warfarin
Allt fler observationella studier baserade på olika register i Europa och USA bidrar nu till kunskaperna om NOAK-behandling (edoxaban är dock för nyligen introducerat för att kunna studeras på detta sätt). Observationella studier är behäftade med störfaktorer (confounding och bias) som kan hanteras mer eller mindre väl i analyserna och de har ett lägre bevisvärde än de experimentella kliniska prövningarna. Ett populärt sätt att minska confounding är att matcha patienterna efter ”propensity score” (för att de jämförda patientgrupper ska ha samma sannolikhet att få de jämförda läkemedlen). Detta medför emellertid att många patienter exkluderas från analyserna. Viktning med covariater eller propensity score (utan matchning) bevarar hela patientmaterialet. Confounding kan aldrig helt undvikas eftersom det kan finnas gömda (icke mätta) faktorer av betydelse och resultaten måste alltid tolkas med försiktighet. Å andra sidan kan resultat från observationella studier vara mer generaliserbara till patienter och behandlingsrutiner i vanlig sjukvård eftersom patienterna i kliniska prövningar är selekterade, välinformerade och bättre uppföljda än i vanlig sjukvård.
I SLL har vi följt samtliga patienter med en icke-valvulär FF-diagnos oavsett vårdnivå (sluten vård, öppen specialistvård eller primärvård) vilket är unikt i sammanhanget. Vi har funnit att persistensen med OAK-behandling (det vill säga fortsatt uthämtning av läkemedlet från något apotek) är mycket god, 88 procent efter ett år och 83 procent efter två år och att den var bättre för warfarin och apixaban än för rivaroxaban eller dabigatran [30]. Vi har undersökt de kliniska utfallen hos samtliga patienter med icke-valvulärt FF som nyinsattes på NOAK (n=9 279) eller warfarin (n=12 919) i SLL under åren 2012–2015 [31]. Resultaten visar en likvärdig strokeprevention med NOAK och warfarin i SLL. Risken att drabbas av ischemisk stroke/TIA eller att dö var likartad med NOAK och warfarin hos patienter med CHA2DS2VASc score ≥2 efter justeringar för obalanser mellan behandlingsgrupperna. Risken att drabbas av allvarlig blödning var också likartad men NOAK-behandling var förenad med färre hjärnblödningar och fler gastrointestinala blödningar. Risken för hemorragisk stroke var halverad men i absoluta tal var inte skillnaden stor (0,2 vs 0,4 procent under det första behandlingsåret, det vill säga en ”number needed to harm” på 500). NOAK var även lika effektiva och säkra som warfarin i vulnerabla subgrupper som patienter ≥80 år och de som haft en tidigare allvarlig blödning. Dosreduktioner var mycket vanligare i SLL än i de stora studierna och förefaller vara adekvata bland de äldre men kanske inte hos yngre patienter. Yngre patienter bör inte dosreduceras utan klara skäl. Mindre skillnader mellan individuella NOAK tolkas med försiktighet på grund av begränsad statistisk styrka och olikheter i patientkarakteristika mellan behandlingsgrupperna i vår studie [31]. Fler svenska studier kommer.
En preliminär rapport från Auricula talar för att NOAK är minst lika effektiva som warfarin (utvalda matchade patienter med TTR ≥70 procent) men ger färre allvarliga blödningar [32]. Friberg preliminärrapporterade färre intrakraniella blödningar men likartad risk för allvarliga blödningar med rivaroxaban jämfört med propensity score-matchade patienter som behandlades med warfarin i en nationell registerstudie (övriga NOAK och strokeutfallen utvärderades ej) [33].
Det finns flera observationella studier från Medicare och andra försäkringsdatabaser i USA, men uppföljningarna av dessa har i allmänhet varit kortare och våra sjukvårdssystem skiljer sig en hel del. Vi fokuserar därför – och av utrymmesskäl – på skandinaviska studier. Från Norge rapporteras att dabigatran och apixaban associeras med färre allvarliga blödningar än rivaroxaban och warfarin, även hos patienter ≥75 år (stroke utvärderades ej) [34]. Från Danmark rapporteras att patienter behandlade med NOAK (endast i standarddos) hade samma strokerisk som warfarinbehandlade patienter men lägre mortalitet och färre allvarliga blödningar med apixaban och dabigatran men ej med rivaroxaban) [35]. Betydelse av skillnader mellan behandlingsgrupperna kan enligt författarna ej uteslutas (så kallad residual confounding). En annan dansk studie rapporterade också likartad strokerisk med NOAK och warfarin samt en lägre risk för intrakraniell blödning med apixaban och dabigatran än med rivaroxaban [36]. I danska registerdata har man funnit fler allvarliga blödningar med rivaroxaban (hazard ratio, HR =1,49), dabigatran (HR =1,17) och warfarin (HR =1,23) än med apixaban [37]; apixaban- och rivaroxabanpatienterna var äldre och hade högre risk score. En dansk studie har fokuserat på dosreducerad NOAK-behandling och fann icke signifikanta tendenser till ökad strokerisk med apixaban 2,5 mg x 2 och minskad blödningsrisk med dabigatran 110 mg x 2 jämfört med warfarin [38]. Man viktade med propensity score men det torde vara problematiskt att jämföra små dosreducerade NOAK-grupper med en stor warfaringrupp där alla har dosjusterad (monitorerad) behandling. Det finns behov av ytterligare och bättre studier avseende dosreducering av NOAK.
Farmakologiska skillnader att beakta vid individuella preparatval
Denna korta sammanfattning av NOAK:s farmakologi baseras på uppgifter i respektive läkemedels aktuella Fass-text [11] och produktmonografi [12-15] samt en ”Practical Guide” från European Heart Rhythm Association, EHRA [39] som uppdaterades 2016 med bland annat mer information om läkemedelsinteraktioner.
Apixaban
Apixaban har en god och ej födointagsberoende biotillgänglighet. Elimineringen är till 1/4 renal och dosreduktion från 5 till 2,5 mg x 2 rekommenderas när minst två av följande kriterier är uppfyllda: s-kreatinin ≥133 µmol/L, ålder ≥80 år eller kroppsvikt ≤60 kg; i praktiken kan eGFR <50 ml/min vara en bättre gräns än ett kreatininvärde vid hänsynstagande till njurfunktionen. Typiska plasmahalter (dalvärden) av apixaban vid dosering enligt FASS finns i Tabell 2 [40,41]. Det finns inga data på relationerna mellan apixabanhalter i plasma och risken att drabbas av stroke eller allvarlig blödning men det förefaller rimligt att hålla sig inom det angivna intervallet för bästa effekt och säkerhet. Apixaban har inte studerats på patienter med eGFR <25 ml/min och denna patientgrupp bör behandlas med stor försiktighet även om gränsen satts till 15 ml/min av läkemedelsmyndigheterna. Det finns ett flertal läkemedelsinteraktioner framför allt via transportproteinet P-glykoprotein (P-gp), men även via läkemedelsmetaboliserande CYP3A4 (se FASS.se och [39]).
Dabigatran
Dabigatran spjälkas från dabigatran etexilat (prodrugformen i Pradaxa) under inverkan av esteraser och har en mycket låg biotillgänglighet (3–7 procent) vilket leder till en hög variabilitet. Det finns en mer än 10-faldig interindividuell variation av dalvärden för dabigatran i plasma med en och samma dosering och dabigatranhalterna var relaterade till stroke och blödning i RE-LY studien [42]. Lämpliga dalkoncentrationer av dabigatran i plasma kan enligt dessa data vara cirka 40–120 ng/ml. Vi har funnit en 20-faldig interindividuell variation av dabigatran i plasma hos patienter som doserats enligt Fass [43] och typiska plasmahalter enligt Tabell 2. En bättre individualisering av doseringarna än enligt riktlinjerna i Fass skulle vara möjlig för dabigatran och vara till nytta för patienterna. Dabigatran elimineras huvudsakligen via njurarna och dess halveringstid ökar påtagligt, med risk för ackumulation, vid sänkt njurfunktion. Doseringen ska sänkas från 150 till 110 mg x 2 vid ålder ≥80 år och vid en samtidig behandling med verapamil. En dossänkning till 110 mg x 2 ska övervägas vid ålder 75–80 år, vid en beräknad eGFR 30–50 ml/min och hos patienter med en ökad blödningsrisk till exempel de med gastrit, esofagit eller gastroesofageal reflux. Vid en kroppsvikt under 50 kg rekommenderas ”noggrann övervakning”; läkemedelsanalys kan vara av värde i denna situation. Regelbunden kontroll av njurfunktionen är viktig och och dabigatran är kontraindicerat i EU vid en eGFR <30 ml/min. Läkemedelsinteraktioner via P-gp [39] ska beaktas vid förskrivning och dabigatran ska ej användas samtidigt med dronedarone. Den vanligaste biverkningen (förutom blödning) är dyspepsi som svarar dåligt på PPI-behandling. Pradaxakapslarna innehåller färgämnen som kan framkalla allergi och de är även fuktkänsliga varför blisterförpackningen ska användas. En specifik antidot (Praxbind) har nyligen introducerats men erfarenheterna av dess användning är ännu begränsade [44].
Rivaroxaban
Rivaroxaban har en god men variabel biotillgänglighet (60 procent i fastande och >90 procent med föda). Intag i samband med måltid rekommenderas för att minska variabiliteten. Medlet doseras x 1 trots att det har en kortare halveringstid än dabigatran och apixaban vilka doseras x 2. Detta medför större svängningar i plasmahalter och effekt under doseringsintervallet (Tabell 2 anger dalvärden) och en större risk för utebliven effekt om doser missas med rivaroxaban jämfört med alternativa NOAK [45]. Engångsdoseringen baserades på studier av patienter med venös tromboemboli och datasimuleringar av FF-patienter; kliniska resultat med edoxaban (se nedan) anses stödja engångsdoseringen med rivaroxaban [46]. Elimineringen är till 1/3 renal och 2/3 hepatisk. Dosreduktion från 20 till 15 mg x 1 rekommenderas vid eGFR <50 ml/min. Rivaroxaban har ej studerats på patienter med eGFR <30 ml/min men har indikation från 15 ml/min. För interaktioner via P-gp och CYP3A4, se Fass.se och [39].
Edoxaban
Edoxaban har en god biotillgänglighet som inte är födoberoende. Elimineringen är till 50 procent renal och 50 procent extrarenal men ej beroende av levermetabolism. Läkemedelsinteraktionerna via P-gp är desamma som för övriga NOAK men andra interaktioner torde bli färre. Medlet doseras x 1 och har en något längre halveringstid än rivaroxaban. I fas II-studier fann man att blödningsrisken var relaterad till dalvärden för edoxaban i plasma och att denna risk blev lägre med endos än med tvådos (se [47]). Trombosrisken utvärderades inte på motsvarande sätt men plasmahalt-effekt data från den pivotala studien har senare publicerats [48]; dessa ger inget underlag för ett ”terapeutiskt fönster” med optimal effekt och säkerhet (såsom för dabigatran [42]). Analysen av edoxaban är ännu inte tillgänglig i SLL. Normaldos är 60 mg x 1 vilken ska halveras enligt kriterierna i Tabell 2. FDA har utfärdat en ”black box warning” att inte behandla patienter med eGFR ≥95 ml/min med edoxaban på grund av bristande strokeskydd [49]. Standardoseringen av edoxaban synes således vara för låg vid normal njurfunktion.
Läkemedelsinteraktioner
Interaktionsproblematiken är mindre med NOAK än med warfarin men samtliga NOAK har läkemedelsinteraktioner som kan höja eller sänka plasmahalter och effekt vid samtidig behandling och som bör beaktas [39,50]. Kunskaperna om interaktioner och dessas kliniska betydelse är emellertid ännu ofullständiga för NOAK. Av särskilt intresse är att antiarytmiska läkemedel som ofta används i behandlingen av FF (dronedaron/amiodaron och icke kärlselektiva kalciumantagonister) höjer halterna av alla NOAK via en P-gp medierad interaktion, samt att starka hämmare eller inducerare av CYP3A4 såsom HIV-läkemedel, svampläkemedel och vissa antibiotika och antiepileptika höjer halterna av FXa-hämmarna. Läkemedelsanalyser (se nedan) är av värde i samband med interaktionsfrågeställningar. För apixaban kan det vara av intresse att notera att resultaten i ARISTOTLE var goda även hos patienter med polyfarmaci [51]. Fass.se och interaktionsdatabasen Janusmed interaktioner [52] uppdateras kontinuerligt. EHRA (www.NOACforAF.eu) har en god information om interaktioner och bedömningar av deras kliniska betydelse [39].
Vikten av god följsamhet
Avbruten antikoagulantiabehandling medför en risk att drabbas av en tromboembolisk komplikation och att dö [53,54]. Följsamhetssiffror från olika studier varierar bland annat på grund av metodologiska problem [55]. Alla direktverkande NOAK har koagulationshämmande effekter som – till skillnad från warfarin – är relaterade till plasmakoncentrationerna varför en utebliven dosering eller ett behandlingsavbrott relativt snabbt leder till utebliven effekt. Det är av stor betydelse att patienterna (gärna även anhöriga) är välmotiverade, välinformerade och införstådda med betydelsen av en god följsamhet. Patienten ska ha en välfungerande vårdkontakt som följer upp behandlingen regelbundet och påminner om betydelsen av regelbunden medicinering samt finns tillgänglig för råd. EHRA trycker särskilt på vikten av att på olika sätt understödja en god följsamhet under NOAK-behandling [39].
Vi har genomfört en första analys av persistens med OAK-behandling i SLL (det vill säga fortsatt uthämtning av läkemedlet från apotek) innan NOAK rekommenderades i Kloka Listan [30]. Vi fann att persistensen var bättre än vad som i allmänhet publicerats från andra regioner och under andra förhållanden [55]. Persistensen med uthämtning av något OAK hos FF-patienter med CHA2DS2VASc ≥2 var 88,2 procent efter 1 år och 82,9 procent efter 2 år. Den var signifikant bättre för apixaban och warfarin än för rivaroxaban och dabigatran. Adherensen (andelen patienter där uthämtningarna kunnat täcka ≥80 procent av behandlingstiden) var också mycket god, 95,7 procent med rivaroxaban, 93,5 procent med apixaban och 92,0 procent med dabigatran (signifikant skillnad mellan rivaroxaban och dabigatran). Vi försökte inte skatta adherensen för warfarin som doseras mycket olika mellan och även varierar inom individer. Förskrivning av OAK från primärvården var associerad med en något bättre persistens än förskrivning från andra vårdgivare. Det är viktigt att dessa initialt mycket goda resultat bibehålls på lång sikt och, om möjligt, förbättras ytterligare genom uppmärksamhet på betydelsen av en god följsamhet.
Litteraturen kring persistens och adherens är mycket varierande, inte minst inom antikoagulantiaområdet [55]. Olika studier har rapporterat adherens/persistenssiffror för NOAK mellan 38 procent och 99,7 procent beroende på variationer i metodik [55]. I Sverige har Friberg rapporterat adherenssiffror för NOAK jämfört med warfarin baserat på nationella register och flera metoder där adherensen för warfarin skattats på basen av doseringsdata från Auricula [56]. I samtliga fall fann Friberg bättre adherens med NOAK jämfört med skattad warfarinadherens. I propensity score matchade analyser var 80 procent täckning av uthämtade mediciner (jämfört med warfarin) 79,5 procent vs 74,3 procent för dabigatran, 91,4 procent vs 73,8 procent för apixaban och 85 procent vs 70,9 procent för rivaroxaban. Persistenserna för warfarin varierade mellan 85,5 procent och 79,7 procent under uppföljningstider som var 1,5–2 år. Dessa data indikerar att NOAK-behandling har skötts väl även i övriga regioner i Sverige. I Danmark har man funnit sämre persistens för dabigatran och warfarin men inte för rivaroxaban jämfört med apixaban [37].
Monitorering
I vissa situationer (akut kirurgi, trombolys vid stroke, planering av interventioner, med mera) är det av stort värde att känna till intensiteten i antikoagulationen hos patienter som behandlas med NOAK såväl som med warfarin. I vissa fall bör även möjligheter att individualisera NOAK-behandling vara av värde (till exempel äldre och/eller njursjuka patienter, patienter med interagerande läkemedel, med mera). Det finns en omfattande erfarenhet av mätning av PK(INR) under warfarinbehandling i olika situationer [2a,57] och det finns många argument för att etablera riktad monitorering även av NOAK [58,59].
Rutinkoagulationstester som PK(INR) och aPTT har litet eller inget värde för bedömning av intensiteten i koagulationshämningen under NOAK-behandling [39,40]. En förlängd aPTT kan spegla en kraftig effekt av dabigatran men en normal aPTT utesluter inte en terapeutisk koncentration av läkemedlet. PK(INR) påverkas endast av supraterapeutiska koncentrationer av dabigatran. APTT lämpar sig inte för monitorering av fXa-hämmarna. PK(INR) påverkas något av fXa-hämning, vilket bör beaktas i samband med skiften till warfarin, men PK(INR)-mätningar saknar värde för monitorering av dessa läkemedel.
Normala till höga halter av dabigatran kan påvisas med ett specialanpassat trombintidstest, Hemoclot TI, medan påvisande av låga halter (till exempel för följsamhetsfrågeställning) erfordrar läkemedelsanalys med LC-MS/MS [59]. För fXa-hämmarna finns särskilda funktionella anti-Xa tester. De mer känsliga och exakta läkemedelsanalyserna med LC-MS/MS finns tillgängliga för dabigatran, apixaban och rivaroxaban men ännu ej för edoxaban.
Funktionella specialtester finns tillgängliga även jourtid på Karolinska universitetssjukhuset medan läkemedelsanalyserna har längre svarstider. För bedömning av testresultat är det av stor vikt att veta när senaste dos togs i förhållande till provtagningen eftersom NOAK:s effekter är direkt relaterade till de fluktuerande plasmahalterna. För dabigatran [42] och edoxaban [48] finns utmärkta data från de stora studierna som relaterar plasmahalter (dalvärden) till effekt och säkerhet.
Behandling av olika patientgrupper
Patienter med mekanisk hjärtklaff eller valvulära flimmer
Patienter med mekanisk hjärtklaff har studerats avseende jämförelse mellan dabigatran och warfarin [60]. Studien fick avbrytas i förtid på grund av bristande effekt av dabigatran trots högre dosering än vid FF och dostitrering med hjälp av plasmakoncentrationer för att försöka uppnå terapeutiska nivåer hos varje patient. Patienter med mekanisk hjärtklaff ska därför behandlas med warfarin! Patienter med hemodynamiskt signifikanta vitier exkluderades ur de pivotala NOAK-studierna varför även patienter med signifikant mitralisstenos i första hand bör behandlas med warfarin.
NOAK vid (el)konvertering
Konvertering av flimmer som ej debuterat inom 48 timmar sker sedan länge efter minst 3 veckors välinställd warfarinbehandling för att minska embolirisken och den ska fortgå minst en månad efter konverteringen (vanligen elkonvertering). Warfarininställningen innebär en fördröjning av åtgärden jämfört med om ett direktverkande NOAK kan användas och det är välkänt att längre flimmerduration inför konvertering ökar risken för flimmerrecidiv. I RE-LY studien genomgick 1 270 patienter 1 983 konverteringar efter minst tre veckors behandling med dabigatran eller warfarin; resultaten var likartade i de jämförda grupperna men studien hade en mycket låg statistisk styrka för att visa likhet (relativ risk för stroke med dabigatran 150 mg x 2 var 0,5 med konfidensintervallet 0,1–2,7 jämfört med warfarin) [61]. I ROCKET AF konverterades 285 patienter under rivaroxabanbehandling [62] och i ARISTOTLE konverterades 743 patienter [63]. Dessa studier under pågående NOAK-behandling är underdimentionerade för värdering av likhet med warfarinbehandling men resultaten var numeriskt lika i de jämförda grupperna. För rivaroxaban finns en studie av nyinsättning innan konvertering som också är kraftigt underdimenionerad men visar numeriskt likartade risker för komplikationer med rivaroxaban och warfarin (två fall av stroke i vardera gruppen) [64]. På Södersjukhuset hade 631 patienter som dabigatranbehandlades inför konvertering goda resultat utan direkta jämförelser med warfarin [65].
NOAK-behandling inför konvertering av FF är nu ett accepterat alternativ till warfarin-behandling [3,4,39] och leder till snabbare åtgärd på grund av den tid det tar att ställa in warfarin eller kontrollera att PK(INR) är adekvat under minst tre veckor hos patienter som redan står på warfarin. Kunskapsunderlaget bör förbättras genom uppföljningar av stora material i sjukvården eftersom ingen adekvat dimensionerad klinisk prövning kan förväntas bli genomförd. Om det, mot förmodan, skulle finnas någon skillnad mellan NOAK och warfarin avseende tromboembolirisk är den liten. När NOAK används inför konvertering är det av största vikt att följsamhet är god under hela behandlingsperioden. Transesofagal ekokardiografi för att utesluta tromb i förmaket är ett beslutstöd vid osäkerhet om följsamheten har varit god. Man bör behandla patienterna minst en månad efter konverteringen oavsett CHA2DS2VASc score och därefter i enlighet med riskskattning med mera [5].
Sköra äldre patienter
Medelåldern var lägre för FF-patienterna i de pivotala NOAK-studierna (70–73 år) än i rutinsjukvården. Exempelvis var endast 13 procent av patienterna i ARISTOTLE ≥80 år [66] medan 36 procent av FF-populationen i SLL är ≥80 år [31,67]. Analyser av ålderns betydelse för behandlingsresultat i NOAK-studierna visar god effekt och säkerhet i höga åldrar men studiepatienterna är selekterade. Våra data från SLL styrker antagandet att NOAK är lika effektiva och säkra som warfarin hos patienter som är 80 år eller äldre [31]. Apixaban var den NOAK som användes mest i den åldersgruppen och har även lägst beroende av njurfunktion för sin eliminering. Apixaban har rekommenderats av ESC för behandling av äldre FF-patienter [68]. Dosreduktioner var mycket vanligare i SLL än i de stora studierna för samtliga NOAK och de föreföll vara adekvata hos patienter ≥80 år [31]
Den största strokebördan bland FF-patienter i SLL 2010 fanns hos de äldre och multisjuka patienter som behandlades med ASA eller inte fick vare sig warfarin eller ASA [67]. SBU har utrett antitrombotisk behandling av äldre och kom fram till att nyttan med behandlingen i de flesta fall torde överstiga riskerna varför man inte ska vara restriktiv med OAK-behandling enbart på grund av hög ålder [69]. Det är således angeläget OAK-behandla även äldre patienter samtidigt som det är viktigt att beakta ”primum non nocere” principen genom goda individuella bedömningar av förväntad nytta i relation till risk.
Patienter med njur- eller leverfunktionsinskränkningar
Av ovanstående framgår att apixaban är den NOAK som har lägst beroende av njurfunktion för sin eliminering. Dabigatran är kontraindicerat vid en eGFR <30 ml/min medan FXa-hämmarna är godkända för användning ner till 15 ml/min. Det är dock klokt att vara restriktiv med behandling av patienter med uttalad njurfunktionsnedsättning (eGFR <25–30 ml/min) eftersom dessa patienter exkluderades ur de pivotala studierna. För samtliga NOAK rekommenderas regelbundna kontroller och beaktande av njurfunktion [39]. Vid beräkning av eGFR bör man betänka att Cockroft-Gault formeln använts i studierna och har legat till grund för doseringsrekommendationer och kontraindikationer; andra formler kan resultera i onödiga överdoseringar [70]. Viktigast är dock att beräkna njurfunktion på något sätt. För mer detaljerad information om NOAK-behandling vid sänkt njurfunktion, se [39]. Läkemedelsanalys kan vara ett stöd för val av dosering hos patienter med sänkt njurfunktion.
NOAK är kontraindicerade vid leversjukdom med koagulationsrubbning. Dabigatrans eliminering är oberoende av leverfunktion men för samtliga NOAK finns inskränkningar i användningen vid leversjukdom se Fass.se och EHRA:s praktiska riktlinjer [39].
Samtidig trombocythämmande behandling vid akuta koronarsyndrom och PCI
Risken för blödning ökar givetvis när antikoagulantia kombineras med trombocythämmande läkemedel. I samband med akuta koronarsyndrom och PCI ges dubbel trombocythämning med ASA och en ADP-receptorhämmare. Det har funnits rutiner för hantering av warfarin, ASA och klopidogrel där trippelterapi givits så kort tid som möjligt och med noggrannare PK(INR)-kontroller. Typ av koronart stent har betydelse för behandlingstiden. Vi avråder från att kombinera OAK-behandling med de mer potenta ADP-receptorantagonisterna tikagrelor och prasugrel. Med NOAK i kombination med dubbel trombocythämning kan problemen öka [71]. Man bör notera att doseringen av rivaroxaban som tillägg till dubbel trombocythämning vid akuta koronarsyndrom är endast 2,5 mg x 2 eftersom högre doser medförde en oacceptabel blödningsrisk [72]. Tillägg av apixaban 5 mg x 2 till trombocythämmande terapi medförde betydligt fler allvarliga blödningar utan att minska risken för kardiella komplikationer efter akuta koronarsyndrom [73]. Tills vidare rekommenderar vi därför en noggrant monitorerad warfarinbehandling före NOAK vid samtidig behandling med ASA och klopidogrel (eventuellt endast klopidogrel).
Hantering av blödningar
Råd om hantering av antitrombotiska läkemedel vid blödningar och inför kirurgi/invasiva åtgärder finns tillgängliga på Janusinfo.se [6] och via SSTH:s hemsida [74]. En översikt om NOAK vid blödning och kirurgi har även publicerats i Läkartidningen [75]. Sedan den skrevs har den specifika antidoten mot dabigatran (Praxbind) tillkommit, se [44].
Värderingar bakom rekommendationerna i Kloka Listan
De aktuella läkemedlen har likartad men inte identisk dokumentation i jämförelse med warfarin men edoxaban har befunnit sig på marknaden endast en kort tid och erfarenheter från vanlig sjukvård saknas. Ur Läkemedelskommitténs och sjukvårdens perspektiv är det viktigt att välja det/de mest ändamålsenliga alternativen när ett bredare utbud står till buds så att de valda läkemedlen blir väl hanterade i sjukvården, med särskilt fokus på primärvården där flertalet patienter med kroniska sjukdomar handläggs. Detta gäller inte minst vid OAK-behandling av FF-patienter där kunskap om läkemedlen behöver finnas i hela sjukvården eftersom dessa patienter är vanliga och handläggs av många doktorer i olika specialiteter.
Apixaban jämfördes med warfarin i ARISTOTLE-studien och har även god dokumentation i jämförelse med ASA i AVERROES-studien. Apixabans överlägsenhet över warfarin i den stora multinationella studien är något överskattad ur ett svenskt perspektiv men medlet är minst lika bra som warfarin även här. ROCKET AF-studien jämförde rivaroxaban med en warfarinbehandling med lägre TTR än de övriga studierna och visade trots detta endast non-inferiority jämfört med warfarin. Endosregimen för rivaroxaban kan ses både som en fördel (enkelhet för patienten) och en nackdel (högre risk för utebliven effekt). Rivaroxaban och dabigatran i doseringen 150 mg x 2 har i jämförelse med warfarin givit upphov till fler allvarliga gastrointestinala blödningar i de pivotala kliniska prövningarna och detta återfinns även i observationella studier. Apixaban är den minst njurfunktionsberoende för sin eliminering bland NOAK. Ett flertal läkemedelsinteraktioner vars kliniska betydelse i många fall ännu inte klarlagts bör dock observeras. Det finns betydelsfulla interindividuella skillnader i plasmahalter vid dosering av apixaban (liksom av övriga NOAK) enligt Fass men underlag för monitorering av FXa-hämmarna för dosjustering finns ännu ej. Mätningar i samband med blödningar är av värde för handläggningen av patienten. FXa-hämmarna saknar ännu specifika antidoter men protrombinkomplex-koncentrat kan förväntas ha effekt (se ovan). Apixaban bedöms vara den lämpligaste FXa-hämmaren att rekommendera.
De observationella studierna visar en likartad bild som de kliniska prövningarna med samma effektivitet för NOAK och warfarin avseende strokeprevention men färre blödningar med framför allt apixaban men även med dabigatran jämfört med warfarin. Samtliga NOAK minskar risken för hjärnblödning jämfört med warfarin vilket är betydelsefullt även om den absoluta skillnaden är liten. SLL-studien ger oss en trygghet i att rekommendera insättning av NOAK-behandling i ökad utsträckning. Detta i kombination med den större komplexiteten med warfarin-behandling gör att vi nu rekommenderar apixaban i första hand i Kloka Listan 2017.
Dabigatran är den NOAK som funnits längst på marknaden (sedan slutet av 2011) varför erfarenheter av behandling utanför studier är störst med detta nya läkemedel. För patienter som är äldre och/eller har sänkt njurfunktion, eller de med dyspeptiska besvär eller med ischemisk hjärtsjukdom är dabigatran mindre attraktivt än FXa-hämmarna. Fördelar med dabigatran är möjligheten att reversera effekten med en specifik antidot och dokumentationen av hur plasmahalter förhåller sig till riskerna att drabbas av stroke respektive allvarlig blödning. Dabigatran har färre läkemedelsinteraktioner än apixaban och rivaroxaban. Det finns skäl att även rekommendera ett NOAK med annan verkningsmekanism. Som fördel bör räknas att två doser av dabigatran (150 mg x 2 och 110 mg x 2) har studerats i en randomiserad prövning medan effektiviteten av apixaban och rivaroxaban i reducerad dos saknar god dokumentation. Dabigatran rekommenderas därför i andra hand jämte warfarin.
Kostnaderna för NOAK är lika (cirka 21 kr/dag; 7 600 kr/år). Läkemedelskostnaden för warfarin är betydligt lägre men kostnader för PK-INR-kontroller tillkommer. Övriga kostnader för en god OAK- och FF-vård tillkommer oavsett preparatval. Det finns ännu ingen hälsoekonomisk värdering av behandlingsalternativen som baseras på kliniska utfall i svensk sjukvård. Ovanstående rekommendationer görs på rent medicinska grunder.
Warfarin rekommenderas nu i andra hand
En välskött warfarinbehandling har fortsatt en viktig roll och den individualiserade doseringen av warfarin genom PK(INR) kontroller är gynnsam för patienter som ej upplever detta som besvärligt. Regelbundna kontroller för optimering av förhållandet mellan riskerna för stroke och blödning kan vara fördelaktigt för vissa patientkategorier och de regelbundna sjukvårdskontakterna bidrar till en god följsamhet. Warfarinbehandling medför en ökad risk för hemorragisk stroke jämfört med NOAK men den absoluta skillnaden är inte stor. Patienter med mekanisk hjärtklaff eller signifikant mitralisstenos ska ha warfarin.
En välfungerande warfarinbehandling ska inte ändras utan goda skäl. I lämpliga fall kan patienterna sköta behandlingen med självmätning eller egenkontroll av PK(INR) (med CoaguCheck) vilket ger mycket bra resultat. Man bör erinra sig att de pivotala NOAK-studierna genomförts med patienter som lämpat sig för warfarinbehandling och att denna behandlings kvalitet (mätt som TTR) haft betydelse för studiernas utfall.
Det finns en omfattande erfarenhet av warfarinbehandling och hur man ska hantera problem kring den. Erfarenheterna av NOAK-behandling utanför strukturerade, väl uppföljda studier är numera också goda. Behandling med NOAK kräver liksom warfarinbehandling en god uppföljning med särskilt fokus på att med noggrann information och eventuella hjälpmedel säkerställa en god följsamhet. Patienterna bör ha ”brickor” som anger att de är antikoagulantiabehandlade och antikoagulantiavarning ska noteras i den elektroniska journalen oavsett preparatval.
Region Stockholms läkemedelskommittés expertgrupp för hjärt- och kärlsjukdomar
Huvudförfattare
Paul Hjemdahl, senior professor/överläkare, ordförande
Klinisk farmakologi, Karolinska universitetssjukhuset Solna
Källa
- Statens beredning för medicinsk och social utvärdering, SBU. Förmaksflimmer. Förekomst och risk för stroke. Rapport 2013
- a) Camm AJ, Kirchhof P, Lip GYH, et al. Guidelines for the management of atrial fibrillation of the European Society of Cardiology. Europace. 2010 Oct;12(10):1360-420
b) Camm AJ, Lip GYH, De Caterina R, et al. 2012 focused update of the ESC Guidelines for the management of atrial fibrillation. Eur Heart J. 2012 Nov;33(21):2719-47 - Kirchhof P, Benussi S, Kotecha D, et al. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur Heart J 2016;37:2893-2962.
- Socialstyrelsen. Nationella Riktlinjer för Hjärtsjukvård
- Stockholms läns läkemedelskommitté. Antikoagulantiabehandling vid förmaksflimmer – lathund 2017 Pdf, 645.6 kB.
- Stockholms läns läkemedelskommitté. Orala antitrombotiska läkemedel vid blödning och inför kirurgi 2017
- Hart RG, Pearce LA, Aguilar MI. Meta-analysis: antithrombotic therapy to prevent stroke in patients who have nonvalvular atrial fibrillation. Ann Intern Med. 2007 Jun 19;146(12):857-67
- Fuster V, Rydén LE, Cannom DS, et al. ACC/AHA/ESC 2006 Guidelines for the management of patients with atrial fibrillation. Eur Heart J 2006;27:1979-2030
- Mant J, Hobbs FD, Fletcher K, et al; BAFTA investigators. Warfarin versus aspirin for stroke prevention in an elderly community population with atrial fibrillation (the Birmingham Atrial Fibrillation Treatment of the Aged Study, BAFTA): a randomised controlled trial. Lancet. 2007 Aug 11;370(9586):493-503
- Connolly SJ, Eikelboom J, Joyner C, et al (for the AVERROES Investigators). Apixaban in patients with atrial fibrillation. N Engl J Med. 2011 Mar 3;364(9):806-17
- Fass.se, Januari 2017
- European Medicines Agency (EMA): Summary of Product Characteristics; Pradaxa.
- European Medicines Agency (EMA): Summary of Product Characteristics; Xarelto.
- European Medicines Agency (EMA): Summary of Product Characteristics; Eliquis.
- European Medicines Agency (EMA): Summary of Product Characteristics; Lixiana.
- Conolly SJ, Ezekowitz MD, Yusuf S, et al (for the RE-LY Investigators). Dabigatran versus warfarin in patients with atrial fibrillation. N Engl J Med. 2009 Sep 17;361(12):1139-51
- Patel MR, Mahaffey KW, Garg J, et al (for the ROCKET AF Investigators). Rivaroxaban versus warfarin in nonvalvular atrial fibrillation. N Engl J Med. 2011 Sep 8;365(10):883-91
- Granger CB, Alexander JH, McMurray JJV, et al (for the ARISTOTLE Investigators). Apixaban versus warfarin in patients with atrial fibrillation. N Engl J Med. 2011 Sep 15;365(11):981-92
- Giugliano RP, Ruff CT, Braunwald E, Murphy SA, Wiviott SD, Halperin JL, et al; ENGAGE AF-TIMI 48 Investigators. Edoxaban versus warfarin in patients with atrial fibrillation. N Engl J Med. 2013 Nov 28;369(22):2093-104
- Douxfils J, Buckinx F, Mullier F, Minet V, Rabenda V, Reginster JY, et al. Dabigatran etexilate and risk of myocardial infarction, other cardiovascular events, major bleeding , and all-cause mortality: a systematic review and meta-analysis of randomized controlled trials. J Am Heart Assoc. 2014 Jun 6;3(3):e000515
- Miller CS, Grandi SM, Shimony A, Filion KB, Eisenberg MJ. Meta-analysis of efficacy and safety of new oral anticoagulants (dabigatran, rivaroxaban, apixaban) versus warfarin in patients with atrial fibrillation. Am J Cardiol. 2012 Aug 1;110(3):453-60
- Ruff CT, Giugliano RP, Braunwald E, Hoffman EB, Deenadayalu N, Ezekowitz MD et al. Comparison of the efficacy and safety of new oral anticoagulants with warfarin in patients with atrial fibrillation: a meta-analysis of randomised trials. Lancet. 2014 Mar 15;383(9921):955-62
- Lip GY, Mitchell SA, Liu X, Liu LZ, Phatak H, Kachroo S, et al. Relative efficacy and safety of non-vitamin K oral anticoagulants for non-valvular atrial fibrillation: Network meta-analysis comparing apixaban, dabigatran, rivaroxaban and edoxaban in three patient subgroups. Int J Cardiol. 2016 Feb 1;204:88-94
- Morgan CL, McEwan P, Tukiendorf A, Robinson PA, Clemens A, Plumb JM. Warfarin treatment in patients with atrial fibrillation: Observing outcomes associated with varying levels of INR control. Thromb Res. 2009 May;124(1):37-41
- Sjögren V, Grzymala-Lubanski B, Renlund H, Friberg L, Lip GY, Svensson PJ, et al. Safety and efficacy of well managed warfarin. A report from the Swedish quality register Auricula. Thromb Haemost. 2015 Jun;113(6):1370-7
- Björck F, Renlund H, Lip GY, Wester P, Svensson PJ, Själander A. Outcomes in a warfarin-treated population with atrial fibrillation. JAMA Cardiol. 2016 May 1;1(2):172-80
- Gómez-Outes A, Terleira-Fernández AI, Calvo-Rojas G, Suárez-Gea ML, Vargas-Castrillón E. Direct oral anticoagulants for stroke prevention in patients with atrial fibrillation: meta-analysis by geographic region with a focus on European patients. Br J Clin Pharmacol. 2016 Sep;82(3):633-44
- Wallentin L, Yusuf S, Ezekowitz MD, et al. Efficacy and safety of dabigatran compared with warfarin at different levels of international normalised ratio control for stroke prevention in atrial fibrillation: an analysis of the RE-LY trial. Lancet. 2010 Sep 18;376(9745):975-83
- Wallentin L, Lopes RD, Hanna M, et al. for the ARISTOTLE Investogators. Efficacy and safety of apixaban compared with warfarin at different levels of international normalised ratio control for stroke prevention in atrial fibrillation. Circulation. 2013 Jun 4;127(22):2166-76
- Forslund T, Wettermark B, Hjemdahl P. Comparison of treatment persistence with different oral anticoagulants in patients with atrial fibrillation. Eur J Clin Pharmacol. 2016 Mar;72(3):329-38
- Forslund T, Wettermark B, Andersen M, Hjemdahl P: Stroke and bleeding with NOAC or warfarin treatment in patients with non-valvular atrial fibrillation: a population based cohort study. Europace 2016; in press. (även presenterat vid ESC Congressen 2016)
- Sjögren V, Bystrom B, Norrving B, et al. Non-vitamin K oral anticoagulants are non-inferior for stroke prevention but cause fewer major bleedings than well-managed warfarin with time in therapeutic range 70 procent or higher in Sweden. American Heart Association 2016 Scientific Sessions. November 13, 2016; New Orleans, LA. Abstract 651.
- Friberg L. Major bleeding among patients with atrial fibrillation treated with rivaroxaban or warfarin in Sweden. Interim results from an on-going post-authorization study. Eur Heart J 2016;37 (Abstract Suppl.):302-403 (Abstract 2067).
- Halvorsen S, Ghanima W, Fride Tvete I, Hoxmark C, Falck P, Solli O, et al. A nationwide registry study to compare bleeding rates in patients with atrial fibrillation being prescribed oral anticoagulants. Eur Heart J Cardiovasc Pharmacother. 2017 Jan;3(1):28-36
- Larsen TB, Skjøth F, Nielsen PB, Kjældgaard JN, Lip GY. Comparative effectiveness and safety of non-vitamin K antagonist oral anticoagulants and warfarin in patients with atrial fibrillation: propensity weighted nationwide cohort study. BMJ. 2016 Jun 16;353:i3189
- Staerk L, Fosbøl EL, Lip GY, Lamberts M, Bonde AN, Torp-Pedersen C, et al. Ischaemic and haemorrhagic stroke associated with non-vitamin K antagonist oral anticoagulants and warfarin use in patients with atrial fibrillation: a nationwide cohort study. Eur Heart J. 2016 Oct 14. pii: ehw496. [Epub ahead of print]
- Lamberts M, Staerk L, Olesen JB, Fosbøl EL, Hansen ML, Harboe L et al. Major bleeding complications and persistence with oral anticoagulation in non-valvular atrial fibrillation: contemporary findings in real-life danish patients. J Am Heart Assoc. 2017 Feb 14;6(2)
- Nielsen PB, Skjøth F, Søgaard M, Kjældgaard JN, Lip GY, Larsen TB. Effectiveness and safety of reduced dose non-vitamin K antagonist oral anticoagulants and warfarin in patients with atrial fibrillation: propensity weighted nationwide cohort study. BMJ. 2017 Feb 10;356:j510
- Heidbuchel H, Verhamme P, Alings M, Antz M, Diener HC, Hacke W, et al. Updated European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist anticoagulants in patients with non-valvular atrial fibrillation. Europace. 2015 Oct;17(10):1467-507
- Skeppholm M, Al-Aieshy F, Berndtsson M, Al-Khalili F, Rönquist-Nii Y, Söderblom L, et al. Clinical evaluation of laboratory methods to monitor apixaban treatment in patients with atrial fibrillation. Thromb Res. 2015 Jul;136(1):148-53
- Al-Aieshy F, Malmström RE, Antovic J, Pohanka A, Rönquist-Nii Y, Berndtsson M, et al. Clinical evaluation of laboratory methods to monitor exposure of rivaroxaban at trough and peak in patients with atrial fibrillation. Eur J Clin Pharmacol. 2016 Jun;72(6):671-9
- Reilly PA, Lehr T, Haertter S, Connolly SJ, Yusuf S, Eikelboom JW, et al. The effect of dabigatran plasma concentrations and patient characteristics on the frequency of ischemic stroke and major bleeding in atrial fibrillation in the RE-LY trial. J Am Coll Cardiol. 2014 Feb 4;63(4):321-8
- Skeppholm M, Hjemdahl P, Antovic J, et al. On the monitoring of dabigatran treatment in "real life" patients with atrial fibrillation. Thromb Res. 2014 Oct;134(4):783-9
- Janusinfo.se. Idarucizumab (Praxbind) – antidot mot dabigatran (Pradaxa)
- Vrijens B, Heidbuchel H. Non-vitamin K antagonist oral anticoagulants: considerations on once- vs. twice-daily regimens and their potential impact on medication adherence. Europace. 2015 Apr;17(4):514-23
- Kubitza D, Berkowitz SD, Misselwitz F. Evidence-based development and rationale for once-daily rivaroxaban dosing regimens across multiple indications. Clin Appl Thromb Hemost. 2016 Jul;22(5):412-22
- Lip GY, Agnelli G. Edoxaban: a focused review of its clinical pharmacology. Eur Heart J. 2014 Jul 21;35(28):1844-55
- Ruff CT, Giugliano RP, Braunwald E, Morrow DA, Murphy SA, Kuder JF, et al. Association between edoxaban dose, concentration, anti-Factor Xa activity, and outcomes: an analysis of data from the randomised, double-blind ENGAGE AF-TIMI 48 trial. Lancet. 2015 Jun 6;385(9984):2288-95
- FDA. Savaysa (edoxaban) prescribing information. 2017-01-30.
- Voukalis C, Lip GY, Shantsila E. Drug-drug interactions of non-vitamin K oral anticoagulants. Expert Opin Drug Metab Toxicol. 2016 Dec;12(12):1445-1461
- Jaspers Focks J, Brouwer MA, Wojdyla DM, Thomas L, Lopes RD, Washam JB et al. Polypharmacy and effects of apixaban versus warfarin in patients with atrial fibrillation: post hoc analysis of the ARISTOTLE trial. BMJ. 2016 Jun 15;353:i2868
- Läkemedelsinteraktionsdatabasen Janusmed interaktioner (tidigare Sfinx)
- Raunsø J, Selmer C, Olesen JB, et al. Increased short-term risk of thrombo-embolism or death after interruption of warfarin treatment in patients with atrial fibrillation. Eur Heart J. 2012 Aug;33(15):1886-92
- Hohnloser SH, Eikelboom JW. The hazards of interrupting anticoagulation therapy in atrial fibrillation. Eur Heart J. 2012 Aug;33(15):1864-6
- Raparelli V, Proietti M, Cangemi R, Lip GY, Lane DA, Basili S. Adherence to oral anticoagulant therapy in patients with atrial fibrillation. Focus on non-vitamin K antagonist oral anticoagulants. Thromb Haemost. 2017 Jan 26;117(2):209-218
- Friberg L. Rapporter till TLV om adherenserna till behandling med dabigatran, rivaroxaban respektive apixaban jämfört med warfarin vid förmaksflimmer i Sverige. November 2015.
- Johnsson H, Stigendal L. Waran och Waranbehandling: en handbok. 2011. ISBN 978-91-633-7557-6. Elektronisk version: www.ssth.se. Tryckt version kan erhållas från Takeda Farma AB.
- Ten Cate H. Monitoring new oral anticoagulants, managing thrombosis, or both? Thromb Haemost. 2012 May;107(5):803-5
- Antovic JP, Skeppholm M, Eintrei J, et al. Evaluation of coagulation assays versus LC-MS/MS for determinations of dabigatran concentrations in plasma. Eur J Clin Pharmacol. 2013 Nov;69(11):1875-81
- Eikelboom JW, Conolly SJ, Brueckmann M, et al. for then RE-ALIGN Investigators. Dabigtran versus warfarin in patients with mechanical heart valves. N Engl J Med. 2013 Sep 26;369(13):1206-14
- Ngarakanti R, Ezekowitz MD, Oldgren J, et al. Dabigatran versus warfarin in patients with atrial fibrillation; and analysis of patients undergoing cardioversion. Circulation. 2011 Jan 18;123(2):131-6
- Piccini JP, Stevens SR, Lokhnygina Y, Patel MR, Halperin JL, Singer DE, et al. Outcomes after cardioversion and atrial fibrillation ablation in patients treated with rivaroxaban and warfarin in the ROCKET AF trial. J Am Coll Cardiol. 2013 May 14;61(19):1998-2006
- Flaker G, Lopes RD, Al-Khatib SM, Hermosillo AG, Hohnloser SH, Tinga B, et al., for the ARISTOTLE Committees and Investigators. Efficacy and safety of apixaban in patients after cardioversion for atrial fibrillation. J Am Coll Cardiol. 2014 Mar 25;63(11):1082-7
- Cappato R, Ezekowitz MD, Klein AL, Camm AJ, Ma CS, Le Heuzey JY, et al; for the X-VeRT Investigators. Rivaroxaban vs. vitamin K antagonists for cardioversion in atrial fibrillation. Eur Heart J. 2014 Dec 14;35(47):3346-55
- Johansson AK, Juhlin T, Engdahl J, Lind S, Hagwall K, Rorsman C, et al. Is one month treatment with dabigatran before cardioversion of atrial fibrillation sufficient to prevent thromboembolism? Europace. 2015 Oct;17(10):1514-7
- Halvorsen S, Atar D, Yang H, De Caterina R, Erol C, Garcia D, et al. Efficacy and safety of apixaban compared to warfarin according to age for stroke prevention in atrial fibrillation: observations from the ARISTOTLE trial. Eur Heart J. 2014 Jul 21;35(28):1864-72
- Forslund T, Wettermark B, Wändell P, von Euler M, Hasselström J, Hjemdahl P. Risks for stroke and bleeding with warfarin and aspirin treatment in patients with atrial fibrillation at different CHA2DS2VASc scores: Experience from the Stockholm region. Eur J Clin Pharmacol. 2014 Dec;70(12):1477-85
- Andreotti F, Rocca B, Husted S, Ajjan RA, Ten Berg J, Cattaneo M, et al. Antithrombotic therapy in the elderly: expert position paper of the European Society of Cardiology Working Group on Thrombosis. Eur Heart J. 2015 Dec 7;36(46):3238-49
- Statens beredning för medicinsk och social utvärdering, SBU. Nytta och risk med läkemedel för äldre: perorala antikoagulantia och trombocythämmare. Rapport 229, 2014.
- Maccallum PK, Mathur R, Hull SA, Saja K, Green L, Morris JK, et al. Patient safety and estimation of renal function in patients prescribed new oral anticoagulants for stroke prevention in atrial fibrillation: a cross-sectional study. BMJ Open. 2013 Sep 27;3(9):e003343
- Verheugt FW. Combined antiplatelet and novel oral anticoagulant therapy after acute coronary syndrome: is three a crowd? Eur Heart J. 2013 Jun;34(22):1618-20
- Mega JL, Braunwald EM, Wiviott SD, et al. for the ATLAS ACS 2-TIMI 51 Investigators. Rivaroxaban in patients with a recent acute coronary syndrome. N Engl J Med. 2012 Jan 5;366(1):9-19
- Alexander JH, Lopes RD, James S, et al. for the APPRAISE-2 Investigators. Apixaban with antiplatelet therapy after acute coronary syndrome. N Engl J Med. 2011 Aug 25;365(8):699-708
- Svenska sällskapet för trombos och hemostas. Kliniska råd vid kirurgi och blödning under behandling med perorala trombocythämmare 2015-11-01
- Dalén M, Hjemdahl P, Holmström M, Ivert T. Blödning och kirurgi vid behandling med nya perorala antikoagulantia; handläggningen kan kompliceras av att specifika antidoter saknas. Läkartidningen 2014;111:274-8
Senast ändrad
